Căutare
Căutare
Toate procedurile
Analiza detaliată
Analiza detaliată
Boala Basedow – Graves (gușa exoftalmică) constă în hiperfuncție tiroidiană difuză, de cauză autoimună, determinată genetic. Este una din principalele forme clinice de hipertiroidie. Aceasta se caracterizează prin tetrada: tireotoxicoză cu hipertrofie tirodiană (gușă difuză toxică), oftalmopatie tiroidiană, mixedem pretibial și acropatia membrelor. Tetrada nu este prezentă întotdeauna, adesea lipsind mixedemul pretibial și acropatia. Incidența bolii este este de aproximativ 1,5 – 2 %, cu un raport femei versus bărbați de până la zece la unul.
În această boală există o stimulare excesivă a tiroidei, independentă de hipofiza anterioară (este cea care secretă TSH), de cauză autoimună. Argumente privind autoimunitatea bolii:
TRAb (anticorpii împotriva receptorului TSH) se leagă de receptorul pentru TSH de pe suprafaţa tireocitelor şi acţionează ca agonişti de tirotropină activând mecanismele care duc la creşterea producţiei şi eliberării de hormoni tiroidieni. Anticorpii îndreptaţi împotriva acestui receptor sunt heterogeni ca natură, astfel că pot avea atât efecte stimulante cât şi inhibitorii, dar per global predomină efectul stimulator.
TRAb sunt detectaţi la aproximativ 90% din pacienţii cu boala Graves netratată. Mai rar, pot fi depistaţi şi la pacenţii cu tiroidită Hashimoto şi la cei cu mixedem primar. Deoarece TRAb aparţin clasei de imunoglobuline G, este posibil transferul placentar de la mamă la făt. Dacă pacientele cu boală Graves prezintă o concentraţie crescută de TRAb în trimestrul al III-lea de sarcină, fătul are risc crescut de a dezvolta hipertiroidie neonatală.
Prezenţa acestor anticorpi este strâns corelată cu activitatea bolii și cu recidiva acesteia. Consecinţele acestei stimulări sunt reprezentate astfel:
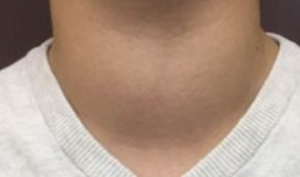
Guşa difuză, omogenă din boala Basedow – Graves
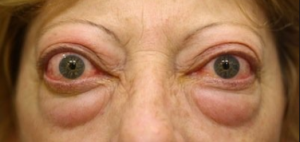
Oftalmopatia din boala Basedow – Graves
Aproximativ 80% din cazurile de oftalmopatie apar în asociere cu hipertiroidismul, deși nu întotdeauna coincid cu debutul hipertiroidiei. În relație cu hipertiroidismul, oftalmopatia o poate precede, poate debuta concomitent cu aceasta sau tardiv, în evoluție.
| Investigația | Modificări induse de tireotoxicoză |
| Hemoleucograma | Microcitoză, policitemie, scăderea conţinutului de hemoglobină, neutropenie, creşterea numărului eozinofilelor şi a limfocitelor, reducerea trombocitelor. |
| Teste biochimice | |
| – glicemia
– colesterol |
– crește
– scade |
| Dozări hormonale | |
| – TSH
– FT4, FT3 |
– scade
– cresc |
| Markerii autoimunitatii tiroidiene: | |
| – anticorpi anti-tiroglobulină şi anti-tiroperoxidază – anticorpi anti – receptori TSH (TRAb) |
– pozitivi (nu sunt specifici)
– pozitivi |
Aceasta oferă posibilitatea de a cuantifica volumul guşii şi relevă un aspect marcat hipoecogen al parenchimului tiroidian (determinat de modificările autoimune – infiltrat limfocitar), iar examinarea Doppler evidențiază hipervascularizația.
Aceasta este mai puţin folosită în prezent pentru diagnosticul bolii Basedow Graves, deoarece aspectul ecografic şi dozările hormonale sunt relevante pentru diagnostic. Scintigrafia este necesară pentru diagnosticul diferenţial cu un adenom toxic (clinic: – guşă nodulară şi hipertiroidie). În boala Basedow scintigrafia relevă o hipertrofie difuză tiroidiană cu hipercaptare difuză a radiotrasorului.
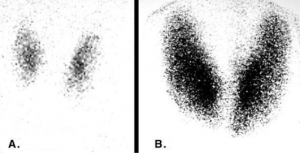
Scintigrafie tiroidiană, A = imagine normală, B = boala Basedow – Graves
Se pot observa pe ECG următoarele modificări:
Tratament igieno – dietetic se bazează pe: evitarea produselor pe bază de iod și evitarea eforturilor fizice şi psihice. Tratament curativ vizează: tratamentul medicamentos cu antitiroidiene de sinteză (de elecție) și tramentul simptomatic (sedative și beta-blocante – ameliorează palpitaţiile, tremurăturile şi semnele neurovegetative), tratamentul cu iod radioactiv și tratamentul chirurgical.
| Antitiroidiene de sinteză = de elecție în boala Basedow – Graves | |
Mod de acțiune |
|
Indicații |
|
Contraindicații |
|
Avantaje |
|
Efecte secundare |
|
Durata tratamentului |
|
Preparate antitiroidiene |
||
Medicament (doză) |
Doza de atac
|
Doza de întreținere (mg pe zi) |
| Tiamazol (5 mg, 10 mg, 20mg) | 10 – 40 | 2,5 – 10 |
| Carbimazol (5 mg, 10 mg, 20 mg) | 15 – 60 | 5 – 15 |
| Propiltiouracil (50 mg) | 150 – 300 | 50 – 200 |
| Perclorat | 1200 – 2000 | 100 – 400 |
| → Doza de atac este de 10 – 40 mg Tiamazol pe zi. După aproximativ trei săptămâni dozele se scad treptat până la cele de întreținere. | ||
Indicații |
|
Contraindicații |
|
Complicații |
|
Doze |
|
Criza tireotoxică, cunoscută astăzi și sub numele de furtună tiroidiană, este o complicație acută, amenințătoare de viață a hipertiroidismului. Aceasta este o prezentare exagerată a tireotoxicozei. Mortalitatea asociată cu furtuna tiroidiană a fost estimată a fi de până la 30% în ciuda progreselor moderne în ceea ce privește tratamentul și măsurile de susținere. Astfel, este foarte important să-l recunoaștem devreme și să începem un tratament agresiv pentru a reduce mortalitatea în aceste cazuri.
Criza tireotoxică este un sindrom rar dar sever caracterizat prin 3 elemente principale: hipermetabolism, alterarea statusului mental și multiple disfuncţii sistemice. Manifestările cardinale ale crizei tireotoxice sunt: febra (frecvent peste 38oC), tahicardie sau tahiaritmie (disproporţionată faţă de febră), manifestări gastrointestinale (de la greaţă şi vărsături până la icter în cazurile foarte severe), manifestări neuropsihice mergând de la agitaţie psihomotorie până la comă. Întrucât nu există un marker biologic şi nici o proporţionalitate între intensitatea manifestătilor clinice şi valoarea hormonilor tiroidieni, diagnosticul crizei tireotoxice se bazează mai mult pe simptomatologia clinică decât pe explorările de laborator. În 80% din cazuri, criza tireotoxică apare la o femeie tânără, cu antecedente personale sau heredo-colaterale semnificative (boli tiroidiene, boli autoimune), după un stres major. Diagnosticul trebuie avut în vedere în faţa instalării bruşte a agitaţiei, febrei, tulburărilor de ritm.
Factorul determinant al crizei este existenţa în antecedente unei tirotoxicoze incomplet tratată sau recent dezvoltată, dar netratată.
Factorii determinanți ai crizei tireotoxice |
|
Factori precipitanți ai crizei tireotoxice |
|
| Factori medicali | Factori chirurgicali |
|
|
Furtuna tiroidiană a început clasic la câteva ore după efectuarea tiroidectomiei (extirparea completă a glandei tiroide) la un pacient pregătit pentru intervenție chirurgicală numai cu iodură de potasiu. Mulți dintre acești pacienți nu au fost într-o stare de eutiroidie înaintea intervenției chirurgicale și deci, nu ar fi pregătiți corespunzător pentru operație, conform standardelor actuale.
Baza fiziopatologică pentru precipitarea furtunii tiroidiene la pacienții cu tirotoxicoză nu este clară. Dar, un factor de precipitare, așa cum sa menționat mai sus, este întotdeauna necesar să provoace furtuni tiroidiene. Furtuna tiroidiană apare cel mai frecvent după o infecție, ceea ce pare să provoace o scăpare din controlul tirotoxicozei. Pneumonie, infecții ale căilor respiratorii superioare, infecții digestive sau orice altă infecție pot provoca această afecțiune.
Nivelul semnificativ crescut al hormonilor tiroidieni nu reprezintă factorul critic al crizei tireotoxice: numeroşi pacienţi cu tirotoxicoză mai puţin severă au nivele comparabile de T4 şi T3. Eliberarea brutală a hormonilor tiroidieni cu schimbarea rapidă a concentraţiilor în fluxul sanguin ar putea explica parţial simptomatologia, fapt susţinut de apariţia crizei postchirurgicale sau la pacienţi care întrerup brusc tratamentul cu antitiroidiene de sinteză sau primesc tratament cu iod radioactiv.
La aceasta s-ar putea adăuga şi faptul că în unele boli severe legarea hormonilor tiroidieni de tiroglobulină scade, crescând fracţia liberă circulantă. Un alt mecanism implicat în patogenia crizei tirotoxice este creşterea receptivităţii periferice la hormonii tiroidieni, întîlnită mai ales în caz de infecţie, acidoză sau hipoxemie.
Majoritatea semnelor şi simptomelor tirotoxicozei severe mimează excesul de catecolamine. Nu este vorba însă atât de o creştere a activităţii catecolaminelor cât de similaritate de acţiune între hormonii tiroidieni şi catecolamine şi de potenţarea activităţii catecolaminelor la nivel celular dependentă de hormonii tiroidieni.
Hipertiroidismul este o stare a excesului de hormoni tiroidieni circulanți care rezultă numai din hiperfuncția intrinsecă a glandei tiroide, în timp ce tirotoxicoza se referă la excesul de hormon tiroidian circulant care provine din orice cauză (inclusiv supradozajul hormonului tiroidian). Manifestarea extremă a tirotoxicozei este furtuna tiroidiană, care se manifestă ca o stare hipermetabolică acută, severă, care pune viața în pericol fie ca urmare a eliberării excesive a hormonilor tiroidieni, determinând hiperactivitate adrenergică, fie modificarea răspunsului periferic la hormonul tiroidian după prezența unuia sau mai multor precipitanți.
Diagnosticul crizei tireotoxice este clinic, o supoziţie forte fiind suficientă pentru instituirea tratamentului, în absenţa căruia prognosticul vital este infaust. La majoritatea pacienţilor cu criză tireotoxică sunt prezente şi accentuate semne clinice ale hipertiroidiei preexistente. Printre simptomatologia clinică a tireotoxicozei preeexistente se numără: guşă difuză sau nodulară, palpitaţii, tahicardie, dispnee, agitaţie, labilitate emoţională, tremor, modificări oculare (retracţie palpebrală, exoftalmie), tegumente calde, umede, fine, fotofobie sau termofobie, scădere ponderală, oftalmopatie, mixedem pretibial. În unele cazuri, tireotoxicoza preexistentă avea o durată medie de șase luni, dar ocazional criza tireotoxică poate apărea şi la pacienţi cu debut recent al hipertiroidiei.
În criza tireotoxică, tabloul clinic este brutal şi dominat de manifestări severe de hipermetabolism. A fost propus un scor clinic bazat pe simptomele specifice şi pe intensitatea lor: temperatura, manifestările neuropsihice, manifestările gastrointestinale şi hepatice, manifestările cardio-vasculare şi factorii precipitanţi. Scorul variază între 0 şi 140, mergând de la tirotoxicoză improbabilă până la tablou foarte sugestiv pentru criză tireotoxică. Recunoaşterea semnelor clinice este esenţială, iar instituirea promptă a tratamentului poate salva viața pacientului.
Simptomatologia clinică cardinală în criza tireotoxică include următoarele elemente:
|
Diagnosticul crizei de tireotoxicoză trebuie bazat pe simptomatologia clinică, explorările funcţionale tiroidiene fiind utile, dar nu definitorii pentru diagnostic !!
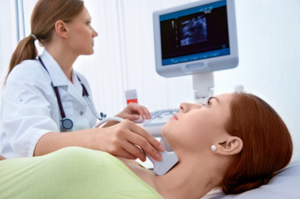
Ecografia tiroidiană
Scorul manifestărilor clinice sugestive pentru o criză tireotoxică |
||
| Criteriu | Scor | |
| Temperatura (oC) | 37 – 38 | 5 |
| 38 – 38,5 | 10 | |
| 38,5 – 39 | 15 | |
| 39 – 39,5 | 20 | |
| 39,5 – 40 | 25 | |
| >40 | 30 | |
| Simptomatologia la nivelul SNC (sistem nervos central) | Absente | 0 |
| Minore (agitație psihomotorie) | 10 | |
| Moderate (delir, psihoză, letargie) | 20 | |
| Severe (obnubilare, comă) | 30 | |
| Simptomatologia la nivelul tractului gastrointestinal și hepatic | Absente | 0 |
| Moderate (diaree, greață, vărsături, dureri abdominale) | 10 | |
| Severe (icter) | 20 | |
| Frecvența cardiacă (bătăi pe minut) | 90 – 109 | 5 |
| 110 – 119 | 10 | |
| 120 – 129 | 15 | |
| 130 – 139 | 20 | |
| >140 | 25 | |
| Prezența insuficienței cardiace congestive | Absentă | 0 |
| Minoră (edeme pretibiale) | 5 | |
| Moderată (raluri subcrepitante bazale bilateral) | 10 | |
| Severă (edem pulmonar acut) | 15 | |
| Fibrilația atrială | Absentă | 0 |
| Prezentă | 10 | |
| Factorii precipitanți (infecţii, traumatisme, cetoacidoza diabetică, embolia pulmonară, pacient incomplet pregătit preoperator pentru chirurgie tiroidiană) | Absenți | 0 |
| Prezenți | 10 | |
Scorul se realizează prin însumarea punctelor obţinute la fiecare criteriu (intervalul posibil: 0 – 140). Înterpretarea scorului este următoarea:
Nu există criterii categorice de diferenţiere a crizei tirotoxice de o hipertiroidie complicată cu altă afecţiune severă (ambele sunt asociate cu febră, tahicardie, diaforeză). Totuşi diferenţierea nu este esenţială, tratamentul fiind acelaşi.
Tratamentul reprezintă o urgenţă medicală şi trebuie instituit înaintea confirmării explorărilor paraclinice privind funcția tiroidiană. Tratamentul furtunii tiroidiene constă în măsuri de susținere precum fluide intravenoase, oxigen, pături de răcire, acetaminofen, precum și măsuri specifice pentru tratarea hipertiroidismului. Dacă sunt prezenți factori de precipitare, de exemplu, infecții, acestea trebuie luate în considerare. Pacienții cu criză tireotoxică trebuie să fie admiși la unitatea de terapie intensive (ATI) cu o monitorizare cardiacă apropiată și un suport ventilator dacă este necesar.
Obiectivele principale în tratamentul crizei tireotoxice sunt:
Antitiroidienele de sinteză, preparate de tionamidă (Propiltiouracil, Metimazol, Carbimazol, Tiamazol), au capacitatea de a inhiba sinteza de T4 şi T3 (blochează organificarea în o oră) dar nu şi eliberarea hormonilor preformaţi. Întrucât nu se găsesc preparate intravenoase, ele trebuie administrate pe per os (pe gură), prin sondă nasogastrică sau pe cale rectală. Administrarea unei doze mari, de încărcare, de îndată ce diagnosticul este pus, permite o îmbunătăţire a simptomelor şi o scădere mai rapidă a tiroxinei:
Când administrarea orală nu este disponibilă, se administrează intrarectal, comprimatele fiind dizolvate în prealabil în ulei mineral. În aceste cazuri, se preferă Propiltiouracil deoarece are şi capacitatea de a inhiba conversia periferică a T4 în T3. Cel mai sever efect advers al tratamentului este agranulocitoza (scăderea masivă a globulelor albe din sânge, în special a neutrofilelor). O leucopenie moderată se întâlneşte frecvent în hipertiroidia netratată şi poate fi majorată de antitiroidiene de sinteză. Acestea nu trebuie întrerupte decât dacă granulocitele sunt < 1000 celule / mm3.
Întrucât tionamidele nu au efect auspra eliberării hormonilor preformaţi în tratament se folosesc substanţe care inhibă secreţia, cum sunt compuşii iodaţi sau carbonatul de litiu.
Iodul (compuşi iodaţi) se administrează la minim o oră după antitiroidienele de sinteză, pentru a se evita utilizarea sa în sinteza hormonilor tiroidieni. Atunci când iodul este administrat după o doză mare de antitiroidiene de sinteză valoarea T4 şi T3 scade semnificativ în câteva zile şi se apropie de normal în 5 – 7 zile. Se folosesc următoarele preparate pe bază de Iod:
Carbonatul de litiu este o alternativă la pacienţii alergici la iod. Poate fi administrat şi înainte de antitiroidienele de sinteză, dar utilizarea sa este limitată datorită toxicității renale şi neurologice. Din această cauză, doza iniţială este de 300 mg la 6 ore, doză care poate fi ajustată cu condiţia ca valoarea Litiului în sânge să nu depăşească limita de 1,5 mEq/L.
Corticosteroizii în doze mari au foat iniţial administraţi pe baze empirice, pentru a combate insuficienţa corticosuprarenaliană. Dozele mari de glucocorticoizi inhibă conversia periferice a T4 în T3. În boala Basedow – Graves ar inhiba direct secreţia de hormoni tiroidieni şi, cel puţin dexametazona, inhibă şi eliberarea hormonilor din tiroidă.
De primă intenție se utilizează Hidrocortizonul, care este administrat într-o doză iniţială de 200 – 300 mg repetate la 8 ore zilnic câteva zile, ulterior dozele fiind scăzute şi înlocuite cu doze echivalente de de medicamente per os. Dintre glucocorticoizii de sinteză se mai utilizează:
Multe efecte periferice ale hormonilor tiroidieni sunt fenomene adrenergice (tahicardia dar şi psihoza, tremorul, diaforeza, diareea etc) putând fi rapid ameliorate prin administrarea de beta – blocante.
Propranololul este cel mai utilizat, cu atât mai mult cu cât determină şi scăderea conversiei T4 în T3. Acest efect apare însă cam după o săptămână, deci nu este util în criza tireotoxică. Propanololul se administrează în doze mari, din cauza severităţii simptomelor şi a ratei crescute a metabolizării şi necesită monitorizarea pulsului, frecvenței cardiace și a tensiunii arteriale. Dozele de Propanolol sunt: 60 – 80 mg la 6 ore, per os sau intravenos 0,5 – 1 mg în 15 minute, apoi 1 – 2 mg la 4 ore (doză maximă 10 mg);
Cele mai semnificative efecte constau în ameliorarea modificărilor cardiovasculare: reducerea rapidă a frecvenţei cardiace, creşterea debitului cardiac, dacă acesta era scăzut din cauza tahicardiei. În insuficienţa cardiacă, Propranololul trebuie administrat cu prudenţă (deşi, dacă insuficienţa cardiacă se datorează disfuncţiei diastolice, scăderea frecvenţei cardiace are un efect salutar). Se preferă o digitalizare prealabilă sau beta-blocante cu acţiune scurtă (labetalol, esmolol). În caz de asociere cu astm bronşic, se utilizează beta1-blocante selective.
Rezerpina, Guanetidina, primele simpaticolitice utilizate în criza tireotoxică, utile în contraindicaţiile beta-blocantelor, sunt mai puţin eficiente şi efecte adverse mai severe – hipotensiune arterială, depresie la nivelul sistemului nervos central – din care cauză în prezent nu mai sunt utilizate.
Îndepărtarea rapidă a excesului de hormoni circulanţi este rezervată cazurilor în care starea clinică se agravează în ciuda tratamentului convenţional al crizei tireotoxice: plasmafereză, dializă și răşini schimbătoare de ioni.
Împachetările (cearşafuri reci, gheaţă, alcool) sunt preferate medicamentelor antipiretice. Ca tratament medicamentos se preferă paracetamolul (se evită salicilaţii care eliberează T4 de pe proteinele transportoare).
Febra şi diaforeza, ca şi vărsăturile şi diareea determină deshidratarea. Corectarea acesteia şi a hipernatremiei se face prin rehidratare pe cale intravenoasă cu ser glucozat 5 – 10%, 3 – 5 L/zi în care se adaugă vitamine din grupul B. Hipercalcemia, dacă este prezentă, se corectează odată cu rehidratarea. La pacienţii vârstnici sau / şi cu insuficienţa cardiacă trebuie evitată supraîncărcarea volemică, pentru a nu agrava insuficiența cardiacă.
Toţi pacienţii cu criză tireotoxică trebuie examinaţi cu atenţie pentru a se identifica o altă afecţiune care ar fi putut favoriza declanşarea crizei. La unii dintre ei (de exemplu, cei care au avut un traumatism) factorul precipitant este evident dar pentru alţii sunt necesare investigaţii suplimentare: formulă leucocitară, glicemie, corpi cetonici, azotemie, radiografie toracică, examenul sputei, uroculturi, hemoculturi).
Odată identificată afecţiunea asociată (cetoacidoză, embolie pulmonară, accident vascular cerebral), aceasta va beneficia de tratamentul specific. Tratamentul cu antibiotice nu este indicat în absenţa infecţiei.
Una din principalele cauze ale crizei tireotoxice este prepararea insuficientă pentru chirurgie. Toţi pacienţii cu hipertiroidie care urmează a fi operaţi, în special cei cu boală Basedow – Graves, trebuie trataţi cu antitiroidiene de sinteză până când se normalizează funcţia tiroidiană (în general, o lună înainte de intervenţia chirurgicală). O alternativă la antitiroidiene de sinteză, pentru boala Basedow – Graves este administrarea de soluție Lugol, care determină şi o scădere a vascularizaţiei tiroidiene.
Tratamentul acesta se administrează în general, circa 2 săptămâni pentru a evita fenomenul de scăpare de sub inhibiţia indusă de iod.
| Dacă tratamentul este urgent, administrarea de antitiroidienelor de sinteză (Propiltiouracil) trebuie începută cât mai repede şi administrat chiar şi în dimineaţa intervenţiei. Prezenţa tahicardiei poate face necesară admnistrarea de beta – blocant intravenous (Propranololul). |
Furtuna tiroidiană este o urgență medicală, o condiție foarte gravă care poate duce la decesul pacienților, dar tratamentul precoce și agresiv poate îmbunătăți rezultatele. Dacă tratamentul este eficient, se observă o ameliorare rapidă a stării generale (în 12 – 24 ore), urmând ca ulterior să apară și ameliorarea agitaţiei, a psihozei (în 72 – 96 ore).
Oftalmopatia (orbitopatia) tiroidiană se referă la complexul de simptome și semne clinice, instalate secundar afectării structurilor orbitare, în boli tiroidiene autoimune. Orbitopatia tiroidiană este cea mai frecventă și mai severă manifestare extratiroidiană a hipertiroidiei autoimmune, boala Basedow – Graves. Rareori se poate întâlni și în tiroidita Hashimoto. Oftalmopatia tiroidiană, prin complicațiile pe care le determină, afectează negativ calitatea vieții pacienților. Calitatea vieții reprezintă un concept multidimensional, care include aspect fizice mentale și sociale.
Sub aspect statistic, incidența anuală a oftalmopatiei din boala Basedow – Graves este estimată la 16 femei și 3 bărbați la 100.000 locuitori. Incidența depinde și de criteriile diagnostice aplicate (clinice, imagistice). Afectarea oftalmică este prezentă la 50% dintre cazurile de boală Basedow – Graves, fiind relevantă clinic la 20 – 30 % dintre acestea. Afectarea subclinică (obiectivată prin computer tomograf sau rezonanță magnetică nucleară) este prezentă la aproximativ 70 % cazuri. Interesarea oftalmică se constată în special la adulții cu vârsta medie de 45 ani, femeile fiind predominant afectate (raportul femei versus bărbățieste de 5 la 1). Oftalmopatia din boala Basedow – Graves se poate întâlni și în patologia tiroidiană autoimună infantilă, unde deține forme mai puțin severe.
Au fost identificați mai mulți factori de risc, cu implicații în apariția și evoluția bolii. Vârsta, sexul, factorii genetici, disfuncția tiroidiană, anumite metode terapeutice (iodul radioactiv), fumatul, titrele anticorpilor față de receptorul TSH (TRAb) sunt cei mai importanți factori de risc. Dacă unii dintre acești factori nu pot fi preveniți, fiind endogeni (de exemplu, vârstă, sex), alții, de ordin exogen, pot fi preveniți (de exemplu, fumat, disfuncție tiroidiană, tratamentul cu iod radioactiv). Intensitatea riscului relative imprimat de factorii enumerați este diferită. Un risc relativ puternic este imprimat de fumat și disfuncția tiroidiană. Sexul, factorii genetici și TRAb conferă bolii un risc mai atenuat.
Procesul patologic intraorbitar include prezența de infiltrate inflamatorii șiun proces intens deadipogeneză. Local, se constată o creștere a producției de glicozaminoglicani (mai ales acid hialuronic), care contribuie prin hidrofilie la hipertrofia structurilor orbitare. Sub aspect patogenic, oftalmopatia din boala Basedow – Graves este rezultanta unui proces autoimun complex. Autoantigenul principal, prezent atât în tiroidă, cât și la nivelul orbitei (fibroblaste, țesut adipos) este reprezentat de receptorul TSH. TRAb-urile sunt îndreptați împotriva receptorului TSH intraorbitar. Secundar activării receptorului TSH, fibroblastele orbitare produc cantități sporite de acid hialuronic, iar o parte dintre acestea se diferențiază în adipocite. Limfocitele T activate, elaborează după interacțiune cu celulele B, citokine proinflamatorii. Citokinele sunt responsabile de extinderea procesului inflamator orbitar. Fenomenele enumerate determină: hipertrofia musculaturii extraoculare, expansiunea țesutului adipos și inflamație orbitară.
Sub aspect fiziopatologic, creșterea volumului conținutului orbitar împinge globul ocular anterior (protruzie, exoftalmie) și impietează circulația venoasă. Afectarea musculaturii extraoculare conduce la diplopie (vedere dublă). Leziunile corneene apar prin mecanisme complexe (lărgirea fantei palpebrale, evaporarea filmului lacrimal, lagoftalmie). Compresiunea nervului optic de către musculatura hipertrofiată la nivelul apex-ului orbitar (neuropatie optică) compromite sever și uneori ireversibil vederea.
Relația temporală dintre disfuncția tiroidiană (hipertiroidism) și oftalmopatie este variabilă. La majoritatea pacienților (85 %), hipertiroidia și oftalmopatia se instalează concomitent (într-un interval de maximum 18 luni). Mai rar, oftalmopatia din boala Basedow – Graves precede instalarea hipertiroidiei sau urmează acesteia. Oftalmopatia din boala Basedow – Graves este bilaterală și asimetrică. La 15 % dintre pacienți, afectarea oftalmică deține caracter unilateral, ridicând importante probleme diagnostice.
Diagnosticul clinic din oftalmopatia din boala Basedow – Graves se bazează pe următoarele criterii:
Majoritatea cazurilor prezintă hipertiroidie (clinică, subclinică), confirmată de valorile TSH-ului și cele ale hormonilor tiroidieni periferici (fracția liberă a hormonilor tiroidieni, T3 și T4). Diagnosticul întampină dificultăți la cazuri cu eutiroidie sau hipotiroidie.
Tabloul imunologic al bolii Basedow – Graves se caracterizează în principal prin prezența unor titre crescute de TRAb-uri. Frecvent sunt sporite și concentrațiile anticorpilor anti – tiroperoxidazici. Prezența TRAb-urilor la cei cu eutiroidie înlesnește stabilirea diagnosticului.
Există numeroase boli oftalmice care prezintă exoftalmie (mai frecvent unilaterală sau marcat asimetrică): tumori orbitare (primare, metastatice), anomalii vasculare (anevrism carotidian, tromboză de sinus cavernos, fistula carotido – cavernoasă), boli granulomatoase, etc.
În cazul unei oftalmopatii din boala Basedow – Graves recent diagnosticate, este obligatorie stabilirea activității și a severității acesteia. Activitatea bolii grevează tipul terapiei. Activitatea unei oftalmopatii din boala Basedow – Graves se referă la prezența fenomenelor inflamatorii, caracteristice fazei inițiale a afecțiunii.
Activitatea bolii poate fi stabilită pe baza unor criterii clinice sau paraclinice. Sub aspect clinic, se evaluează scorul de activitate clinică, definit de șapte simptome și semne clinice. Acestea sunt reprezentate de următoarele:
→ Fiecare simptom sau semn este cuantificat cu 1. → În cazul unui scor de activitate clinică ≥ 3, se apreciază că boala este activă. |
Activitatea bolii poate fi evaluată la cazuri selecționate și cu ajutorul ecografiei orbitare, a rezonanței magnetice nucleare orbitare sau a scintigramei orbitare cu Octreotid (captarea octreotidului este intensă în faza activă a afecțiunii). Severitatea oftalmopatiei din boala Basedow – Graves se referă la simptomele și semnele induse de afectarea cronică a structurilor orbitare. Pentru stabilirea severității bolii este necesară evaluarea fantei palpebrale, a afectării țesuturilor moi (conjunctivă, pleoape), a importanței exoftalmiei si a disfuncției musculaturii extraoculare. Disfuncția musculaturii extraoculare determină diplopie de diverse grade (intermitentă, inconstantă și constantă). Alte semne de severitate importantă sunt induse de interesarea corneei sau a nervului optic.
Din punct de vedere al severității, oftalmopatia din boala Basedow – Graves recunoaște: forme ușoare (40%), forme cu severitate medie (33%) și forme severe (28%). Formele foarte severe sunt determinate de ruptura de cornee, neuropatia optică și interesează 3 – 5 % cazuri.
Investigațiile imagistice orbitare (tomografia computerizată, rezonanța magnetică nucleară) nu sunt obligatorii la toate cazurile. Acestea se recomandă în: oftalmopatii marcat asimetrice (15 – 20% dintre pacienți), la cei fără hipertiroidie, în suspiciune de neuropatie optică și înaintea practicării intervențiilor pe orbită. Metodele imagistice evidențiază interesarea structurilor orbitare, respectiv musculature extraoculară, exoftalmia, ponderea țesutului fibroadipos.
Istoria naturală a oftalmopatiei din boala Basedow – Graves recunoaște mai multe faze și anume:
Dacă manifestările inflamatorii cedează în timp, exoftalmia, retracția palpebrală și disfuncția musculaturii extraoculare persistă, devenind cronice.
Cea mai importantă complicație a oftalmopatiei din boala Basedow – Graves este reprezentată de neuropatia optică. La majoritatea cazurilor este determinată de compresiunea nervului optic de către musculature extraoculară hipertrofiată, la nivelul apexului orbitar. Din punct de vedere clinic, debutul este insidios cu disconfort ocular important, vedere încețoșată, afectarea simțului cromatic, scăderea acuității vizuale și defect pupilar.
Tratamentul oftalmopatiei din boala Basedow – Graves cuprinde măsuri profilactice și măsuri curative, adaptate activității și severității afecțiunii.
La toate cazurile este necesară tratamentul profilactic, adică sistarea fumatului (încetinește evoluția bolii, reduce severitatea exoftalmiei și a diplopiei, sporește eficiența medicației imunosupresoare) și corectarea disfuncției tiroidiene (hipertiroidie, hipotiroidie iatrogenă). Tratamentul hipertiroidiei vizează obținerea eutiroidiei prin antitiroidiene de sinteză, tiroidectomie (totală) și mai puțin prin tratamentul cu iod radioactiv. Indiferent de măsura terapeutică folosită, este necesară corecția cât mai precoce a unei hipotiroidii iatrogene. Terapia cu iod radioactiv deține anumite riscuri, reprezentate de agravarea oftalmopatiei preexistente sau apariția acesteia de novo. Iodul radioactiv se poate administra la cazuri selecționate, cu respectarea anumitor precauții (asociere de corticosteroizi, tratarea hipotiroidiei).
În forma ușoară a bolii, se aplică măsuri profilactice, măsuri locale (lacrimi artificiale, prisme pentru corecția diplopiei) și medicație antioxidantă (Pentoxifilină 1200 mg pe zi, preparate de Seleniu 200 µg pe zi, timp de 12 luni). Monitorizarea pacienților se face la trei – șase luni prin examen clinic, oftalmologic și testarea funcționalității tiroidiene.
Forma moderată a bolii ridică uneori probleme terapeutice. Există mai multe posibilități terapeutice.
Se aplică cazurilor cu debut recent (sub un an) active (scorul de activitate clinică ≥ 3). Glucocorticoizii se pot administra oral (doză de atac 40 – 100 mg pe zi, cu reducere progresivă timp de 10 – 24 săptămâni). Deși tratamentul nu este lipsit de eficiență, poate conduce la efecte secundare importante. Glucocorticoizii administrați intravenos ca puls – terapie recunosc mai multe scheme terapeutice. În general, se recomandă Metilprednisolon 500 mg pe zi, intravenos, o dată pe săptămână, timp de șase săptămâni, apoi 250 mg, o dată pe săptămână, alte șase săptămâni).
Tratamentul este mai eficient (cu răspuns terapeutic prompt la aproximativ 80 % cazuri), iar efectele secundare mult mai reduse. Contraindicațiile pentru corticosteroizi sunt reprezentate de: hepatita recentă, disfuncția hepatică, hipertensiunea arterială, diabet zaharat decompensat, osteoporoza, tulburările psihice și glaucomul.
Se prefera la cei cu tulburări severe ale motilității oculare. Un răspuns terapeutic adecvat se constată la 60% cazuri. Contraindicațiile sunt reprezentate de: diabet zaharat cu retinopatie diabetică, vârstele sub 35 ani (risc carcinogenetic pe termen lung). Monitorizarea cazurilor cu severitate medie se face, indiferent de terapia aplicată, la trei și șase luni.
Forma severă a bolii (neuropatia optică) impune tratament de urgență cu doze mari de glucocorticoizi intravenos. Se administrează Metilprednisolon 1 g pe zi intravenos, timp de trei zile în prima săptămână, repetându-se aceeași schemă în a doua săptămâna. Dacă parametrii oftalmici se ameliorează, se poate continua cu corticoterapie per os. Dacă nu se constată o ameliorare, se practică decompresiune orbitară.
Forma inactivă de oftalmopatie beneficiază de chirurgie reabilitativă, care se aplică la șase luni de la inactivarea bolii. Există o ierarhizare a procedurilor chirurgicale, începându-se cu decompresiune orbitară, urmată de chirurgia strabismului și in final de cea a pleoapelor. Un tratament corect, o bună aderență a pacienților și o monitorizarea adecvată a cazurilor îmbunătățește semnificativ calitatea vieții pacienților.

Dislipidemia , Nefropatia diabetica , Sindromul insulinic autoimun cu hipoglicemie Neuropatia diabetica
© Copyright 2025 NewsMed - Toate drepturile rezervate.