Căutare
Căutare
Toate procedurile
Analiza detaliată
Analiza detaliată
 Durerea este un fenomen complex psiho-social determinat de interacțiunea unor sisteme multiple neuroanatomice și neurochimice cu variate procese cognitive și afective. IASP (International Association for the Study of Pain) defineşte durerea ca „o senzaţie şi o experienţă senzitivă şi emoţională neplăcută asociată cu o leziune tisulară existentă sau potenţială, sau descrisă ca o astfel de leziune„.
Durerea este un fenomen complex psiho-social determinat de interacțiunea unor sisteme multiple neuroanatomice și neurochimice cu variate procese cognitive și afective. IASP (International Association for the Study of Pain) defineşte durerea ca „o senzaţie şi o experienţă senzitivă şi emoţională neplăcută asociată cu o leziune tisulară existentă sau potenţială, sau descrisă ca o astfel de leziune„.
Studiile efectuate în ultimii ani au fost îndreptate asupra determinării capacității copiilor de a simți, de a exprima sau raporta și de a-și aminti durerea suferită. Rezultatele obținute au arătat că percepția durerii nu este dependentă de gradul mielinizării, iar căile de conducere a durerii sunt formate înaintea nașterii, chiar din a 28-a săptămână de gestație, astfel că, nou – născuții și sugarii simt intens durerea și chiar își pot aminti experiențele dureroase. Mai mult, datorită lipsei influenței căilor inhibitorii descendente, nou-născuții, sugarii și copiii mici experimentează durerea chiar mai puternic decât adulții.
În lipsa posibilităților de verbalizare, recunoaștea și evaluarea durerii la acești copii se realizează în prezent prin tehnici unanim acceptate, clasificate în următorele categorii: observații comportamentale, măsurători fiziologice. De asemenea, există metode care folosesc măsurători complexe (comportamentale și fiziologice) cu ajutorul cărora estimarea durerii este mult mai precisă.
Concepții greșite cu privire la durerea copilului |
|
Este important să se obțină controlul durerii la nounăscut și sugar atât pentru comfortul acestuia cât și pentru prevenirea consecințelor imediate și la distanță. Aceste consecințe au efecte dăunătoare asupra întregii stări de sănătate a individului. Este cunoscut faptul că cel de al III-lea trimestru de sarcină reprezintă perioada critică privind organizarea sistemului nervos. În consecință, în această etapă a dezvoltării sistemului nervos, nou-născuții prematuri sunt cei mai vulnerabili la acțiunea factorilor vătămători. Prin urmare, supunerea acestor nou – născuți la proceduri dureroase repetate în serviciile de terapie intensivă neonatală determină modificarea pragului de durere, a percepției și a toleranței la durere pe tot parcursul vieții persoanei respective.
În descrierea durerii, o serie de termeni utilizați frecvent sunt:
Cum am amintit mai sus, conform Asociației Internaționale pentru Studiul Durerii durerea reprezintă o experiență senzorială și emoțională neplăcută asociată leziunilor tisulare actuale și potențiale. În urma injuriei, fiecare persoană își formează propria imagine asupra durerii, iar interpretarea acestor experiențe este subiectivă și evaluarea durerii se bazează pe metode de auto-relatare. Desigur, această definiție nu poate fi aplicată ușor în toate situațiile, în particular nou-născuților, sugarilor și copiilor mici care nu-și pot verbaliza durerea. În plus, răspunsul acestora la durere nu este prea diferit de cel al fricii și suferinței apărute ca urmare a situațiilor nedureroase. Astfel, sfera definiției durerii poate fi lărgită prin includerea noțiunilor de suferință și stres. Dacă durerea este întotdeauna stresantă, stresul nu este în mod necesar dureros.
Realizarea unui control adecvat al durerii nou-născuților presupune cunoașterea unor concepte importante și anume:
Un alt factor important care conduce la creșterea sensibilității la durere a prematurilor este reprezentat de faptul că, în timp ce transmiterea durerii este bine dezvoltată, mecanismele de modulare a durerii sunt imature, conducând la alterarea abilității acestora de a lupta cu impulsurile nociceptive primite. Există o întârziere a dezvoltării căilor descendente inhibitorii din ariile supraspinale, întârziere a maturației interneuronilor din substanța gelatinoasă și o posibilă deficiență a neurotransmițătorilor inhibitori. Prin urmare, neurotransmițătorii excitatori care sunt din belșug la naștere, pot să nu fie echilibrați printr-un număr adecvat de neurotransmițători proveniți din căile descendente inhibitorii. Această modulare scăzută a durerii determină creșterea excitabilității în cornul dorsal al măduvei spinării și, ca urmare, crește sensibilitatea la durere.
O metodă sensibilă pentru evaluarea pragului la durere este reprezentată de răspunsul flexor cutanat la stimularea dureroasă. Pentru a testa acest reflex, stimulul noxic este aplicat pe planta piciorului și se măsoară pragul de retracție în flexie. S-a mai constatat că prematurii au un prag al durerii foarte scăzut sesizat și la aplicarea firului de păr von Frey pe suprafața plantară a piciorului. Firul von Frey este un monofilament de nylon suficient de rigid pentru a fi aplicat cu forță pe piele. Manevra conduce la realizarea reflexului de retracție în flexie. Pragul de durere crește corespunzător cu vârsta.
Nevoia ameliorării durerii la prematur este importantă datorită efectelor dăunătoare ale durerii cu consecințe generale asupra perioadei de sugar. Resursele energetice de care are nevoie nou-născutul pentru creștere și vindecare sunt folosite pentru învingerea durerii. Întregul răspuns la durere are drept rezultat creșterea frecvenței cardiace și respiratorii, creșterea presiunii sanguine și eliberarea hormonilor adrenali de stres.
Tulburarea ciclului somnului, ca rezultat al durerii, determină consecințe imediate și la distanță. Sistemele neurologice care controlează atenția, emoția și starea de somn – veghe interacționează la nivel cerebral. Ca urmare, stresul și durerea care conduc la întreruperea repetată a ciclului somnului pot afecta neurodezvoltarea copilului și există chiar riscul apariției deficitelor de atenție și ale tulburărilor emoționale. Răspunsurile la durere determină creșterea presiunii intracraniene și tulburarea dinamicii diafragmatice care conduc la creșterea volumului sanguin intracranian. Aceste modificări au drept rezultat creșterea incidenței hemoragiilor intracraniene și a leucomalaciei periventriculare la prematuri, urmate de leziuni neurologice.
După cum am menționat, la naștere sunt prezente toate structurile neurologice și neurotransmițătorii necesari transmisiei și interpretării impulsurilor dureroase. Căile durerii continuă însă să se dezvolte în perioada de sugar și copil. Vulnerabilitatea crescută a creierului la efectele dăunătoare ale durerii este datorată atât faptului că la naștere dezvoltarea creierului este într-o perioadă critică cât și creșterii ulterioare rapide a acestuia.
La nou-născut există o densitate mare a receptorilor NMDA în jurul cornului dorsal al măduvei spinării cât și în zonele supraspinale iar în urma activării receptorilor NMDA se constată o creștere a influxului ionilor de calciu. Prin stimularea prelungirilor fibrelor C nociceptoare se eliberează neurotransmițătorul glutamat care acționează pe receptorii NMDA din măduva spinării. Creierul tânăr este susceptibil la excitotoxicitatea indusă de NMDA. Doi cercetători au emis ipoteza că procedurile dureroase repetate efectuate asupra prematurilor activează excesiv aminoacizii excitatori și receptorii NMDA, afectând dezvoltarea neuronilor.
Efectele asupra dezvoltării neuronilor includ scăderea pragului de sensibilizare, fenomenul de „windup“ și de sensibilizare centrală. Prin sensibilizare centrală se înțelege că neuronii măduvei spinării devin mult mai sensibili la toate impulsurile primite. Studii recente sugerează că mecanismele mediate NMDA sunt susceptibile de a produce stare de durere cronică persoanelor care au experimentat durerea în mod repetat.
Studiile susțin că stimularea dureroasă repetată la nou-născuți conduce la hiperinervație, cu înmugurirea fibrelor de durere atât A cât și C. Această înmugurire este parțial datorată unei creșteri a aprovizionării cu factor de creștere nervoasă, care este mult mai disponibil la nou-născut decât la copii și adulți. Un studiu pe șobolan nou-născut cu pielea piciorului rănită a demonstrat înmuguriri îndelungate ale terminațiilor nervoase senzoriale care au condus la hiperinervație și scăderea pragului de durere chiar după vindecarea rănii. Autorii atribuie acest fenomen de hipersensibilizare plasticității sistemului nervos al sugarilor foarte mici cât și efectelor durerii asupra fibrelor senzoriale aflate în perioada critică de dezvoltare nervoasă. Hipersensibilizarea prelungită descrește pragul de durere până la punctul la care prematurul poate percepe stimuli, care în mod normal sunt nedureroși, cum ar fi mânuirea acestora, ca fiind stimuli dureroși.
Există tot mai multe dovezi că atât fătul cât și nou – născutul sunt capabili să experimenteze durerea. Cercetările inițiale în această chestiune au fost îndreptate asupra răspunsului diferențiat al hormonilor de stres în timpul intervențiilor chirurgicale efectuate sub analgezie sau anestezie opioidă sau neopioidă. Controlul efectuat în timpul procedurilor chirurgicale în două studii de referință, fără să se determine tipul analgeziei și anesteziei, a indicat existența unei revărsări a hormonilor de stres, cu efect clinic dăunător asupra sugarilor ce au primit control minim al durerii sau cărora nu li s-a administrat tratament.
Studiile ulterioare efectuate asupra leziunilor tisulare actuale datorate procedurilor dureroase au înregistrat: creșteri semnificative ale frecvenței cardiace, frecvență cardiacă variabilă, o descreștere a tonusului vagal și a saturației în oxigen.
Aceasta crește ca răspuns la un stimul dureros acut. Rata creșterii frecvenței cardiace variază în mod obișnuit de la 10 bătăi pe minut până la 20 – 25 bătăi pe minut. Nu în toate situațiile au fost înregistrate creșteri ale frecvenței cardiace, ci uneori, în special la prematuri, ca răspuns la durerea acută a fost notată bradicardia. De exemplu, intubația, pe lângă faptul că este o manevră dureroasă, stimulează de asemenea țesutul visceral influențând frecvența cardiacă. Unii sugari nu manifestă modificări ale frecvenței cardiace și nu răspund la nici o procedură dureroasă sau, uneori, răspunsul este minim. În concluzie, frecvența cardiacă poate să nu fie cel mai consecvent indicator al răspunsului la durerea acută, în ciuda utilizării obișnuite.
Alt indicator cardiovascular care a fost folosit în evaluarea durerii la sugar a fost reprezentat de variabilitatea frecvenței cardiace ca răspuns la înțeparea călcâiului sau la strângerea acestuia după incizie.
Este un indicator mult mai precis al răspunsului simpatic respirator și cardiac la durere, descrescând după înțeparea călcâiului, circumcizie și injecție.
Măsurată de obicei transcutanat, saturația perifică a oxigenului a fost raportată mai rar ca mod de răspuns la acțiunea durerii, dar când este determinată se constată că nivelul său este scăzut. Ca răspuns la stimularea dureroasă acută, unele cercetări au raportat un nivel al descreșterii la 80% atât la nou – născuții la termen cât și la prematuri. În studiile în care nivelul oxigenării determinat transcutanat nu a scăzut atât de abrupt, s-a avut în vedere că a existat posibilitatea ca sugarii să fi fost asistați ventilator, astfel că procentul de oxigen inhalat a fost crescut în timpul efectuării procedurilor și, ca urmare, a compensat desaturarea. Totuși, această ajustare însă nu a fost reflectată corespunzător în măsurătorile efectuate.
Măsurată la sugari prin transpirația palmară și plantară, conductibilitatea cutanată este o reflectare a stimulării sistemului nervos simpatic și este deci un indicator al stării de veghe și de stres. Când s-a folosit la sugari, cercetătorii au constatat că testul nu a fost concludent pentru sugarii cu vârstă mai mică de 37 de săptămâni, datorită modului imatur de producere a sudorii.
Se determină prin manevre neinvazive folosind senzori plasați pe fontanela anterioară. Presiunea intracraniană este o măsurare indirectă a fluxului sanguin cerebral, iar fluctuațiile largi pot avea drept rezultat diferite sechele neurologice. Ambele măsurători pot fi folosite ca indicatori ai răspunsului la procedurile invazive. Creșteri ale valorilor au fost raportate ca răspuns la intubație, aspirație și înțeparea călcâiului.
Totuși sunt mulți factori care influențează presiunea intracraniană și fluxul sanguin cerebral, inclusiv plânsul sau simpla deschidere a izoletei. Măsurarea fie a presiunii intracraniene cu senzor de presiune din fibră optică sau determinarea fluxului sanguin cerebral prin ultrasonografie Doppler sau prin spectroscopie infraroșie presupune echipamente speciale care nu sunt disponibile în serviciile clinice, deși ar fi utile cercetării în scopul înțelegerii răspunsului fiziologic al sugarului la durerea acută.
Răspunsurile comportamentale la durere reflectă în general încordarea întregului corp, înclusiv ale căilor vocale, corpului și feței. Comportamentele examinate sunt: plânsul, mișcările corpului și expresia facială.
A fost adesea folosită ca indicator al durerii, considerându-se că o durată mai mare a plânsului indică o intensitate mai mare a durerii. Cercetătorii care au încercat să urmărească caracteristicile plânsului au notat că „țipătul de durere“ este cu grad mai înalt și mai strident decât plânsul datorat foamei, frustrării sau sperieturii. Totuși, această constatare nu este consecventă. Într-un studiu în care au fost examinate eșantioane acustice ale plânsului ca răspuns la analgezie, s-a remarcat că nu există diferențe ale trăsăturilor plânsului deși există diferențe ale incidenței plânsului. În concluzie, se poate considera că nu caracteristicile plânsului, ci cantitatea plânsului reflectă durerea acută a sugarului.
Mișcările faciale care realizează grimasa, sunt interpretate ca expresie a situațiilor dureroase. Expresia facială a fost intens studiată fiind considerată un indicator sigur și constant al răspunsurilor comportamentale la durere. Expresiile faciale ale nou-născutului, care experimentează durerea acută, include următoarele caracteristici:
Pentru prematurii foarte mici a căror musculatură facială nu este suficient dezvoltată sau care prezintă aparatură aplicată pe față (de exemplu, tuburi sau benzi de înregistrare), unele mișcări faciale sunt obscure vederii. În această situație, prezența de trei mișcări faciale superioare singure (sprâncene proeminente, strângerea ochilor, cuta nasolabială) sunt considerate suficiente pentru a deosebi durerea de situațiile nedureroase.
Mișcările corpului ca încordarea și / sau mișcările de lovire ale membrelor. Un studiu a demonstrat că nou – născutul lovește puternic cu piciorul neafectat piciorul al cărui călcâi a fost supus înțepăturii, localizând astfel durerea. Grunau și colaboratorii au efectuat un studiu comparând mișcările corpului prematurului ca răspuns la manevrele de invazivitate diferită (de exemplu, schimbarea de pampers și aspirarea endotraheală). Acești cercetători atrag atenția că numai extensia membrelor inferioare și evazarea degetelor sunt mișcări care indică durerea, în timp ce agitarea și răsucirea torsului apar ca răspuns la manevre mai blânde sau apar chiar spontan.
Prin urmare, cercetătorii au constatat că atât nou – născutul la termen cât și prematurul pot să distingă durerea față de alte experiențe tactile, iar țipătul și expresia facială rămân modalitățile cele mai obișnuite de exprimare a durerii. De menționat că răspunsurile prematurilor la durere sunt mai puțin viguroase decât ale nou – născuților la termen; semnele sunt mult mai subtile incluzând plânsul mai slab, grimase mai puțin pronunțate, iar poziția este moale, flască, indiferentă.
Studiile s-a raportat că sugarii care sunt supuși unor intervenții chirurgicale răspund la durere pe o perioadă de timp de peste 30 de minute până la câteva zile. Indicatorii care au fost utilizați în studiu au fost: răspunsul hormonal, modificările comportamentale și reflexul cutanat în flexie.
Stresul hormonal, în particular descărcarea de cortizol și catecolamine (determinate în mod obișnuit: epinefrina și norepinefrina) au fost urmărite ca răspuns după intervenția chirurgicală pe cord deschis și după chirurgie generală la sugarii născuți prematur sau la termen, și după circumcizie la sugarii născuți la termen. Cortizolul a fost studiat în proceduri mai puțin laborioase, cum ar fi aspirarea endotraheală sau în îngrijirea de rutină a sugarului.
Aceste substanțe sunt legate de stress, dar nu totdeauna de durere. Totuși, când sugarii bolnavi născuți prematur au primit un opioid sintetic – meperidina, pentru aspirație endotraheală – nivelurile de cortizol au fost mult mai puțin crescute. Mai mult, la cei supuși intervențiilor chirurgicale care au primit doze mari de opiod intraoperator și doze mari postoperator, s-au înregistrat creșteri semnificativ mai reduse ale cortizolului. Bazat pe constatările studiilor privind răspunsul hormonal în transmiterea datelor durerii, pare că aceste substanțe sunt legate de starea de veghe și/sau stres, iar nivelurile acestora sunt modificate semnificativ numai de agenți analgezici majori (de exemplu, opioidele).
Testează sensibilitatea periferică fiind un indicator al durerii. Pragul durerii, urmărit prin reflexul cutanat în flexie, când călcâiul sugarului a fost supus unei incizii, a fost ridicat prin folosirea de anestezice topice aplicate pe zona tăiată.
Este influențată de capacitatea sugarului de a relaționa pozitiv cu părinții sau cu persoanele care îi îngrijesc cât și cu mediul înconjurător. Dacă starea de plâns poate reflecta durerea, prezența unor perioade lungi de somn presupune stare de comfort a sugarului. Creșterea perioadei de somn liniștit a fost inclusă ca modalitate de evaluare a prezenței sau absenței durerii.
Sugarii percep durerea pe aceleași căi ca cele ale adulților. Receptorii pentru stimulii nociceptivi sunt terminațiile nervoase libere care sunt în mare măsură distribuite pe toată suprafața corpului. Ca urmare, ele sunt prezente în special în straturile superficiale ale pielii dar, de asemenea, în țesuturile interne cum ar fi periostul, peretele arterial și suprafața articulațiilor.
Stimulii mecanici, chimici sau termici excită nociceptorii, iar impulsurile sunt transmise cornului dorsal al măduvei prin două grupe de fibre nervoase și anume, fibrele mielinizate A-delta și fibrele nemielinizate C. Pe calea tractului spinotalamic, constituit în principal din axonii neuronilor laminari I, IV și V ale cornului posterior, impulsurile sunt transmise către talamus unde este percepută durerea. Proiecțiile acestuia din cortexul senzorial și din ariile bazale ale creierului influențează probabil aprecierea calității durerii și componenta afectivă.
Căile neuronale sunt modulate de neurotransmițători care au rolul de a amplifica sau de a atenua transmisia impulsurilor. Componenta emoțională și afectivă este modulată prin experiența anterioară și prin memorie. Substanța cenușie periapeductală și regiunea mezencefalică periventriculară se comportă ca un sistem analgezic inerent. Din aceste regiuni, semnalele sunt transmise prin nucleii din punte și din trunchiul cerebral către cornul dorsal al măduvei spinării, blocând senzația de durere. Neurotransmițătorii implicați în suprimarea durerii sunt opiodele endogene care includ beta-endorphinele, encephalinele și dinorphina. Alți neurotransmițători, cum ar fi serotonina și acidul gama-amino-butiric (GABA) au, de asemenea, rolul să diminue senzația de durere.
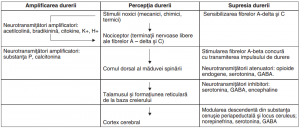
În concluzie, diferențele de bază în neurofiziologia percepției durerii la nou-născut și sugar sunt reprezentate de faptul că impulsurile nociceptive sunt conduse către măduva spinării, în principal, prin fibre nemielinizate decât prin fibre mielinizate și există, de asemenea, o relativă paucitate a neurotransmițătorilor inhibitori în ele. Sugarii au în plus un câmp receptor pentru durere mai întins și posibil există o concentrare mai mare a receptorilor substanței P. De asemenea, ei au prag mai scăzut la impulsul de excitare și sensibilizare, astfel că, la stimularea nociceptivă sunt percepute mai multe efecte centrale. Se consideră că acești factori determină ca sugarul să simtă durerea mult mai intens decât persoanele cu vârstă mai mare.
Nou – născuții și sugarii nu-și pot comunica durerea prin cuvinte. În absența auto-raportării se utilizează diverși indicatori în scopul de a determina locul, natura și severitatea durerii. Durerea este asociată cu modificări fiziologice, biochimice, comportamentale și psihologice care pot fi înregistrate și cuantificate.
Răspunsurile sugarului la durere |
||
Modificări fiziologice |
Modificări comportamentale |
Modificări biochimice |
Creșteri ale:
|
Modificări ale expresiei faciale:
|
Creșterea descărcării de:
|
Modificări autonome:
|
Mișcări ale corpului:
|
Scăderea secreției de: |
Prin măsurarea parametrilor fiziologici s-a constatat o creștere cu până la 20% ca răspuns la durere. Aceste modificări sunt secundare secreției de cortizol și catecolamine, iar aceste substanțe sunt cele care stau la baza succesiunii clasice „luptă sau fugi“ a copilului mare și adultului. Este relativ ușor să se determine alterarea parametrilor fiziologici fără utilizarea unor echipamente invazive. Aceste măsurători asociate cu unele răspunsuri comportamentale reprezintă indicatori foarte sensibili în determinarea durerii la sugar.
Dintre modificările comportamentale, expresia facială a sugarului reprezintă indicatorul cel mai stabil și cel mai sigur, fiind considerat „etalonul de aur“ pentru evaluarea durerii la această grupă de vârstă. Deși modificările biochimice sunt probabil cei mai sensibili parametri cuantificabili, au dezavantajul major de a putea fi determinate prin metode invazive. Din acest motiv, ele nu sunt folosite de rutină pentru evaluarea percepției durerii. Există unele dovezi că prin combinarea rezultatelor modificărilor fiziologice și comportamentale se furnizează o mai bună estimare a durerii sugarului. În scopul de a introduce obiectivitate în evaluarea durerii sugarului, au fost desemnate și validate diferite scale ale durerii. Ele se bazează fie pe variațiile parametrilor fiziologici, fie pe determinarea modificărilor comportamentale sau pe combinarea acestora.
Metodele multidimensionale care includ observații comportamentale și cuantificări ale parametrilor fiziologici cuprind scalele CRIES (acronim pentru plâns, modificarea saturației oxigenării transcutanate, frecvența cardiacă, presiunea sanguină, expresia facială și alterarea tipului de somn) și PAT. Scala Profilul Durerii la Nou Născutul Prematur este o modalitate de evaluare a durerii procedurale la nounăscutul prematur și include șapte indicatori (comportamentali, fiziologici și contextuali). La început scala Profilul Durerii la Nou Născutul Prematur a fost folosită pentru prematurii mai mari de 28 săptămâni de gestație, iar ulterior scala a fost validată pentru determinarea eficienței intervențiilor nefarmacologice la prematuri. Scala CRIES menționată mai sus, se aplică sugarilor și chiar copiilor care nu comunică, iar scorul este semnificativ pentru durere când este peste 4. Cuprinde următoarele determinări care sunt notate astfel:
→ Plâns
→ Respirație – necesită supliment de oxigen pentru menținerea saturației oxigenului peste 95%
→ Înregistrarea frecvenței cardiace și a presiunii arteriale:
→ Expresia facială:
→ Somn:
Trebuie subliniat că durerea nu este determinată numai de proceduri invazive, ci chiar de unele acțiuni simple cum ar fi scoaterea benzii lipite, comprimarea membrului pentru menținerea unei poziții, modificări posturale în timpul ventilației sau prin manevre de fizioterapie.
Situații clinice în care sugarii experimentează durerea |
||
Condiții de boală |
Proceduri de diagnostic |
Proceduri terapeutice |
| • otita medie;
• faringite și infecții ale cavității orale; • afte ulcerate; • dureri toracice asociate tusei; • colicile sugarului; • dureri de cap; • leziuni tisulare datorate traumatismului; • hidrocefalia; • sângerări intracraniene; • enterocolita necrozantă; • spasticitatea; • tromboflebita. |
• puncția călcâiului;
• puncția venoasă și arterială; • puncția suprapubiană a vezicii; • puncția lombară; • puncția ventriculară; • aspirația endotraheală; • bronhoscopia; • paracenteza toracică; • aspirarea lichidului de ascită; • endoscopia gastrointestinală; • cistoscopia. |
• canulă intravenoasă;
• injecție intramusculară; • cateterismul ombilical; • introducerea sau scoaterea sondei nasogastrice; • cateterismul vezicii urinare; • intubația endotraheală; • aspirarea; • circumcizia; • schimbarea pansamentelor rănilor; • proceduri de incizie și drenaj; • stări postoperatorii; • introducerea și scoaterea tubului de drenaj; • scleroterapie endoscopică. |
Durerea este o experiență cu efecte adesea benefice prin atenționarea organismului asupra unei injurii actuale sau iminente, chiar impiedicarea apariției sau limitarea unor leziuni. Cu toate acestea, durerea are și efecte distrugătoare prin acțiunea asupra metabolismului cât și asupra răspunsurilor comportamentale.
Efectele durerii asupra sugarului |
||
Efecte imediate |
Efecte pe termen scurt |
Efecte pe termen lung |
| • iritabilitate;
• frică; • tulburarea somnului și stării de veghe; • creșterea consumului de oxigen; • dezechilibru ventilație / perfuzie; • diminuarea aportului nutrițional; • creșterea acidității gastrice. |
• creșterea catabolismului;
• alterarea funcției imunologice; • întârzierea vindecării; • scăderea legăturii emoționale. |
• memoria durerii;
• retard în dezvoltare; • alterarea răspunsului la experiențele dureroase următoare. |
Pe termen lung, memoria experiațelor dureroase au influență atât asupra percepțiilor dureroase următoare cât și asupra răspunsului la durere. O dovadă în acest sens este reprezentată de studiile clinice clasice prin care este demonstrată diferența răspunsului la vaccinare a sugarilor care au fost supuși circumciziei sub anestezie față de cei operați fără anestezie. Există de asemenea unele dovezi că experiența durerii neonatale poate să aibă efecte îndepărtate chiar până la vârsta preșcolară sau mai mult.
Influențe multiple, incluzând factori legați de sugar cât și unele caracteristici ale persoanelor care îi îngrijesc, contribuie împreună la dezvoltarea unor asemenea evenimente. Din punctul de vedere al persoanelor care îngrijesc nou – născuții și sugarii, durerea are două consecințe importante. Prima este neîncrederea celor mici față de cei care îi îngrijesc, generată de eșecul prevenirii sau ameliorării durerii. În al doilea rând, inadecvata analgezie pentru procedurile inițiale poate scădea efectul terapeutic la doze analgezice adecvate pentru procedurile următoare.
În principal, controlul durerii sugarului se bazează pe trepiedul:
Există o largă varietate de strategii privind controlul durerii, de tehnici de evaluare, de protocoale standardizate privind dozele, regimurile și căile de administrare ale tratamentului. În continuare, am să enumăr strategile de bază considerate importante de a fi urmărite în scopul controlului durerii sugarului:
Medicamentele antiinflamatoare nesteroidiene sunt în general folosite pentru tratarea durerii de intensitate mică și ca supliment în scopul reducerii dozei totale de opioizi. Numai unele din aceste medicamente au fost studiate la sugarii mici. Ele pot fi valabile în situațiile în care se cere ameliorarea durerii pentru o perioadă mai lungă de timp și unde există riscul inducerii dependenței opioide. Recent, unul din cele mai populare antiinflamatoare nesteroidiene, Nimesulid, a fost interzis de a fi utilizat la copii datorită efectelor hepatotoxice potențiale.
În clinică, se recomandă folosirea unei combinații raționale de analgezice în diferite proporții pentru obținerea celor mai bune rezultate cu cele mai reduse efecte secundare.
Cea mai potentă clasă de medicamente analgezice este cea a opioidelelor, incluzând Morfina, Metadona, Oximorfina, Codeina, Fentanil, Alfentanil și Sufentanil. Aceste medicamente au în plus efect sedativ și anxiolitic. Alt avantaj relativ al acestui grup este că în situația unui supradozaj efectele sunt ușor reversibile. Cu toate acestea, ele pot determina toleranță și dependență, efecte pe termen lung care nu au fost studiate la nou-născuți și sugari. De asemenea, ele au perioadă de înjumătățire variabilă care depinde adesea de vârsta gestațională a pacientului și ca urmare influențează doza și frecvența administrării acestora.
Înaintea utilizării sistemice a oricărui medicament analgezic sau anestezic la sugari, trebuie să fie studiate proprietățile farmacocinetice și farmacodinamice ale acestora, deoarece mânuirea acestor medicamente se face diferit la sugari față de adulți. În plus, starea clinică a sugarilor trebuie înțeleasă în întregime, cu referire specială la capacitatea acestuia de a metaboliza și de a excreta medicamentul.
Sugarii mici, în special nou-născuții cu greutate mică la naștere și prematurii, sunt imaturi privind capacitatea de metabolizare a medicamentelor și astfel, este necesar ca medicamentul să se administreze în doze reduse sau să se crească intervalul dintre administrări. Alt aspect care trebuie urmărit înaintea administrării acestor substanțe este tipul de medicație pe care sugarul o primește deja pentru afecțiunea clinică, pentru a nu se produce interacțiuni medicamentoase nedorite.
Agenții anestezici locali blochează transmiterea impulsurilor de la receptori către măduva spinării. Teoretic vorbind, ei pot fi administrați pe oricare dintre cele trei căi, și anume: prin infiltrarea locală a substanței, prin blocarea nervului sau prin blocarea regională intravenoasă. Ultimele două metode necesită un grad ridicat de experiență tehnică și prin urmare, pot să nu fie realizabile în timpul diagnosticului de rutină sau al executării procedurilor terapeutice.
Infiltrarea sigură și eficientă a medicamentelor anestezice locale a fost bine documentată pentru efectuarea procedurilor chirurgicale scurte cum ar fi circumcizia cât și pentru executarea unor proceduri în scop diagnostic cum ar fi aspirarea măduvei osoase, biopsii, etc. Cu toate acestea, infiltrarea locală cu substanțe anestezice nu este larg utilizată din două motive majore.
Primul este riscul real sau presupus de apariție a efectelor secundare la substanțele anestezicelor utilizate, care includ anafilaxia, hipotensiunea și alte efecte mai puțin severe. Acestea sunt riscuri care desigur trebuie să fie luate în considerare. Totuși, cea mai obișnuită motivație este probabil tentația medicilor de a executa procedurile „repede introdus, repede scos“ și astfel ,,cruțarea“ sugarului de două înțepături de ac. Asemenea atitudini trebuie să fie descurajate energic, în special dacă durerea infiltrației anestezice locale poate să fie minimalizată substanțial sau chiar evitată prin folosirea acelor disponibile mai subțiri, special pentru infiltrație, neutralizând pH la anestezicul local, încălzind anestezicul la temperatura corpului înainte de a fi folosit prin injectarea cât mai lent posibil.
Un amestec eutactic (în proporții egale) de 2,5% Lidocaină și 2,5% Prilocaină denumit EMLA (amestec eutactic de anestezice locale) a devenit tot mai cunoscut. Combinația eutactică este o mixtură a celor două medicamente anestezice locale în proporție egală de 1:1. Aplicat cu aproximativ 60 minute înaintea procedurii intenționate, el penetrează până la o profunzime de 5 – 10 mm, furnizând o analgezie bună pentru câteva minute. Penetrarea poate să fie crescută prin aplicarea unui bandaj ocluziv pe suprafața unsă. Totuși, EMLA nu trebuie să fie folosită pe suprafețe lezate sau pe mucoase. Dezavantajele majore ale EMLA sunt vasoconstricția și riscul de methemoglobinemie.
Un amestec de Tetracaină, Ametocaină și Cocaină (prescurtate TAC) este un alt anestezic local cunoscut în unele părți ale globului.
Există medicamente cu efecte reduse analgezice și anestezice, dar folosite ca auxiliare analgezicelor, pentru eficacitatea lor sedativă și / sau analgezică. Ele nu înlocuiesc analgezicele, ci suprimă unele din răspunsurile comportamentale asociate durerii. Prin monitorizarea corespunzătoare a frecvenței cardiace și respiratorii cât și prin determinarea saturației transcutanate a oxigenului, acești agenți pot fi folosiți în mod avantajos.
Există intervenții care sporesc activarea sistemului descendent inhibitor și prin urmare determină scăderea percepția durerii. Atenuarea transmiterii impulsurilor către măduva spinării poate fi obținută prin stimularea fibrelor nervoase senzoriale groase care mediază sensibilitatea tactilă și cea de cald – rece. Intervențiile nefarmacologice pot, de asemenea, să moduleze sensibilizarea și răspunsul la durere prin modificarea atenției și scăderea senzației de frică.
Intervenții nefarmacologice pentru ameliorarea durerii sugarului |
|
Trebuie resubliniat că intervențiile nefarmacologice practicate izolat nu par să amelioreze durerea. Ele sunt mai folositoare numai ca strategii complementare metodelor farmacologice de ameliorare a durerii acute. Intervențiile nefarmacologice atrag atât prin ușurința de a fi folosite cât și prin faptul că nu necesită monitorizare. Deși nu există efecte adverse raportate prin utilizarea acestor metode, publicațiile au subliniat că utilizarea repetată de sucroză pentru analgezia nou – născuților mai mici de 31 de săptămâni vârstă gestațională, poate să-i supună unui risc privind dezvoltarea neurocomportamentală din următoarele săptămâni de viață.
Principiul de bază privind modificarea tehnicilor operaționale este să reducă incidența și frecvența stimulilor care pot fi percepuți de către pacient ca stimuli noxici. Acestea cuprind:
Adesea, o modificare a practicilor poate ajuta la reducerea durerii la nou – născuți și sugari. De exemplu, sugarii arată semne mai reduse de durere în timpul puncției călcâilui când se folosește incizie mecanică comparativ cu incizia manuală. De asemenea, practicarea puncției venoase în vederea recoltării probelor de sânge este raportată a fi mai puțin dureroasă decât puncționarea călcâiului. La fel poate fi considerată inserția cateterului venos central la sugarii care necesită recoltare frecventă de sânge, față de puncțiile repetate venoase sau ale călcâiului. Bineînțeles, o asemenea opțiune trebuie să fie cântărită în lumina duratei de așteptare până la denudare cât și a riscului de infecție și de tromboză. Cu toate acestea, există dovezi care arată că rata infecției la nou – născuții denudați central nu este mai mare decât al celor supuși puncțiilor multiple.
Există unele situații în care durerea este prezentă pe o perioadă îndelungată de timp, fie ca episoade scurte repetate, fie ca fenomen continuu. O asemenea situație este întâlnită la sugarul cu o malignitate. În aceste cazuri, scopul ameliorării durerii este să furnizeze maximum de comfort pentru perioade lungi de timp. Din acest motiv sunt preferate medicamente analgezice și anestezice cu durată de acțiune lungă și cu efecte secundare sistemice minime. Butamben este un agent anestezic local care injectat epidural poate produce blocare senzorială pentru câteva luni. Un avantaj în plus este protejarea neuronilor motori deși, acest aspect este controversat în prezent.
O metodă alternativă de creștere a duratei activității anestezice poate fi reprezentată de folosirea preparatelor anestezice locale cu eliberare lentă. Există unele progrese față de preparatele cu liposomi și constau în eliberarea treptată a microsferelor conținând anestezic local. Altă opțiune poate fi considerată blocarea plexului nervos sau chiar ablația folosind alcool sau fenol; se presupune că este eficientă pentru un interval de până la șase luni. Metoda de instilare a substanțelor analgezice prin cateterul epidural și pe cale intratecală, de asemenea, este o tehnică subapreciată.
Organizația Mondială a Sănătății a sugerat un protocol care cuprinde patru pași abordați gradat în controlul durerii în cancer. Acesta implică începerea cu analgezice non – opioide, apoi folosirea opiodelor orale, urmată de folosirea parenterală a opioidelor puternice și în cele din urmă se recurge la aplicarea tratamentului cel mai invaziv cum ar fi administrarea intratecală sau epidurală a medicamentalor, blocarea nervoasă, etc.

Dislipidemia , Nefropatia diabetica , Sindromul insulinic autoimun cu hipoglicemie Neuropatia diabetica

Bronșita acută , Infectia cu citomegalovirus la copil , Infectii urinare la copii Răceala la copii
© Copyright 2024 NewsMed - Toate drepturile rezervate.